在近期自身免疫性脑炎的检测中,我们遇到一系列具有明确脑炎表现的患者,其初始检测结果具有典型共性:常规CBA(包括 NMDA、LGI1、CASPR2、AMPAR、GABAA/B、DPPX 等)均为阴性。但TBA呈现高度一致的神经丝样染色模式。TBA的“神经丝型”模式在文献中具有明确指向性(Neurology 2018)。正是这一发现,引导我们进一步拓展检测至NIF(neuronal intermediate filament)抗体谱系,最终确诊NFH(neurofilament heavy chain)抗体阳性。这提示TBA阴性或可疑模式不是结果的终点,而是下一步拓展检测的重要“导航信号”。那么,为什么初始CBA阴性,却能通过TBA识别线索?因“初筛范围”而非“技术缺陷”。
本病例并非因为CBA 技术缺陷或抗原构象依赖组织环境。而是因为初始 CBA 并未覆盖 NFH/NIF系列抗原,这是目前多数临床实验室的常态。在我国的AE抗体检测体系中,NIF(α-internexin、NfL、NfM、NfH)尚未进入常规筛查项目。因此初筛CBA阴性并不代表患者无免疫性病因,通过TBA特征性染色模式指向拓展NIF系列,最终NFH被检测出阳性。
这种“TBA →拓展→确证”的模式,在罕见抗体的诊断中尤为重要。
既往研究中(Neurology 2018)中,Mayo Clinic明确描述了NIF抗体的两大组织染色模式(图1):(1)分布于小脑颗粒层—浦肯野层—分子层的纤维状染色,对应:α-IN、NfL、NfM(2)主要集中在浦肯野层周围的粗纤维状染色,对应NfH。我们描述的病例中TBA 的染色模式与文献中的NFH模式一致,使拓展方向明确。
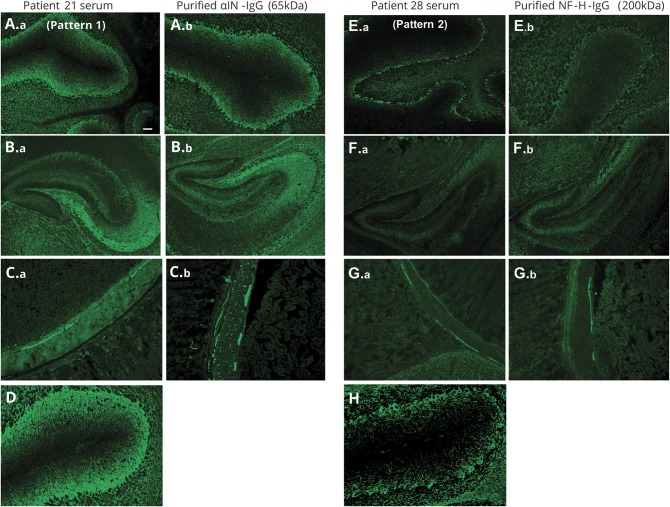
图1 患者免疫球蛋白 G(IgG)与小鼠组织结合的免疫荧光模式(Neurology 2018)。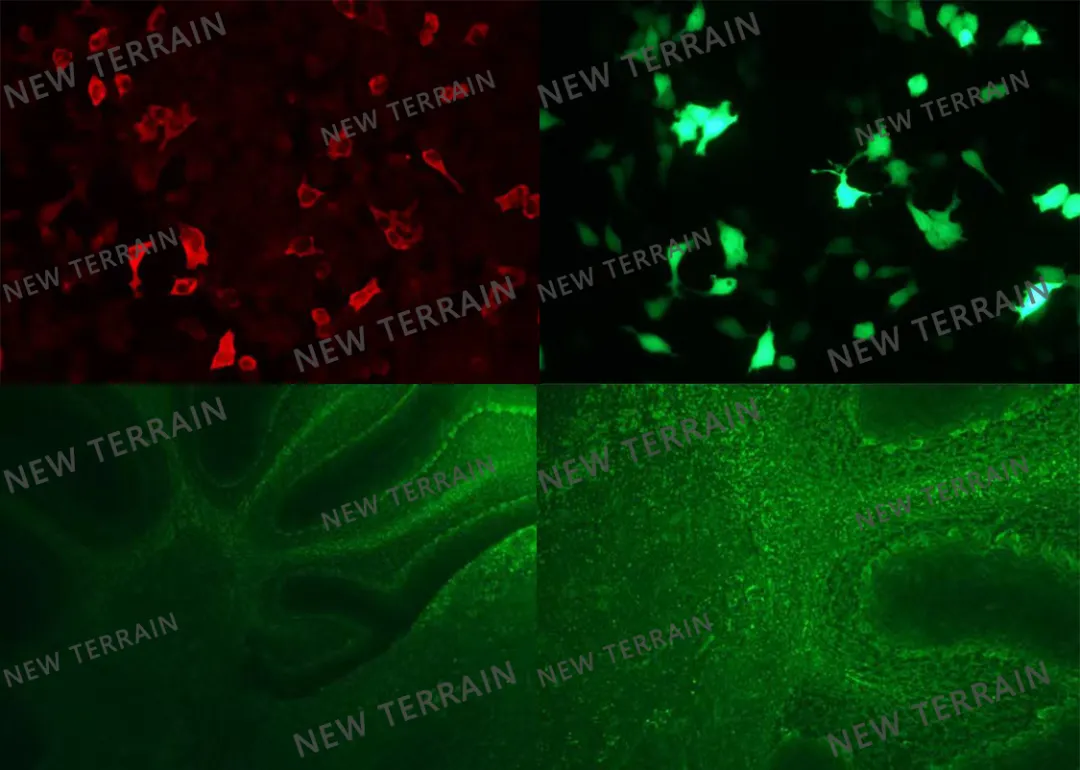
图2 患者CBA和TBA结果图(天海新域)
NFH抗体属于NIF-autoimmunity 体系,其特征为:神经系统受累广泛,包括小脑共济失调,脑病/认知下降,脊髓炎,外周神经病,这些均符合神经丝损伤的解剖学分布。虽然肿瘤相关性低于NfL,但仍需警惕。NfL抗体阳性的肿瘤检出率高达 77%(多为神经内分泌肿瘤),而NFH单阳性者肿瘤相关率明显更低。但文献仍建议NFH阳性患者应至少完成一次全面肿瘤筛查。免疫治疗多数有效,文献中多例 NIF 抗体患者在应用类固醇、IVIG 或 PLEX 后均明显改善。
从本次病例可见,TBA 带来的价值主要体现在:
(1)指导拓展方向。TBA的“神经丝样”模式 指向NIF抗体,用CBA法进一步验证最终确定NFH阳性。(2)弥补初筛抗体 panel 的不足。目前临床常规CBA并不包含NIF系列,TBA是发现这些抗体的重要窗口。(3)避免漏诊罕见但具有临床意义的抗体。NFH若未检测,将导致临床病因不明,错失免疫治疗时机,肿瘤监测缺乏依据。(4)形成分层诊断路径:首先常规CBA阴性,其次TBA阳性(非特异或神经丝样),若符合既往文献明确的染色模式,进行相关抗体的拓展筛查,最终建立诊断与治疗路径。
TBA在自身免疫性脑炎诊断体系中的不可替代性NFH虽不是最常见的 AE 抗体,但其阳性对于诊断、治疗与随访具有重要指向意义。未来,我们需要:
1. 常规脑炎panel阴性并高度疑似AE的患者必须进行TBA检测。
2. 出现“神经丝样”染色时,应立即拓展NIF系列检测。
3. NFH 阳性后应结合临床、影像与肿瘤筛查进行综合评估。
天海实验室目前已推出两种神经丝蛋白抗体检测产品,供临床选择